V дегеніміз вакцина
Иммунитеттің қызметі неде? Вакциналар қалай жұмыс істейді? Әртүрлі вакциналар арасындағы айырмашылық қандай? Вакциналар сіздің ДНК-ңізді өзгертеді ме?
Шамамен осыдан бір жарым жыл бұрын ақпан айының соңында біз «Сіз коронавирусты жұқтыруыңыз мүмкін» деген мақаланы аудардық. Оның негізгі ойы — коронавирусты жұқтырмаудың мүмкін еместігі және ол адамзатпен тұмау сияқты ұзақ жылдар бойы бірге болатын маусымдық ауру болуы мүмкін, ал коронавирустық инфекциялармен күресудің жалғыз құралы вакцина болады деген идея.
Міне, \(2021\) жылдың маусымында бізде вакцина бар, бірақ егілушілер саны көбірек бола алар еді. Бірден атап өтетіні: егер сіз вакцинация мемлекеттердің, трансұлттық корпорациялардың және (немесе) Билл Гейтстің қастандығы екеніне шүбәсіз сенсеңіз, онда сіздің бұл бетті жабуыңызға болады. Мен сізбен салғыласқым келмейді. Неліктен? Бірдеңені түсінбеуіңіз мүмкін деген кішкене ықтималдықты өзіңіз мойындап, оның мүмкін екендігіне жол бергеңізге дейін сізді ешкім сендіре алмайды.
Бірақ негізгі әңгімеге оралсақ, бұл мақалада мен иммундық жүйеге қысқаша шолу жасаймын, әртүрлі вакциналардың қалай жұмыс істейтінін түсіндіремін және кейбір мифтер мен қате түсініктерді түсіндіруге тырысамын.
Иммундық жүйе қалай жұмыс істейді?
Иммундық жүйе соншалықты үлкен және әртүрлі, сондықтан оның толық сипаттау үшін бөлек мақаланы арнаған дұрыс. Бірақ қысқаша шолу жасап өтсек болады, тіпті қажет десек қателеспеспіз.
Иммундық жүйе өзінің және бөгде жасушалардың дифференциациясына негізделген. Біздің жасушаларымыз жақсы және біз оларға қол тигізбейміз, бірақ бейтаныс жасушалар көзден алшақ болуы керек. Бұл бірден екі сұрақ тудырады:
№1. Кім өзіңдікі, кім өзге екенін қалай түсінсек болады?
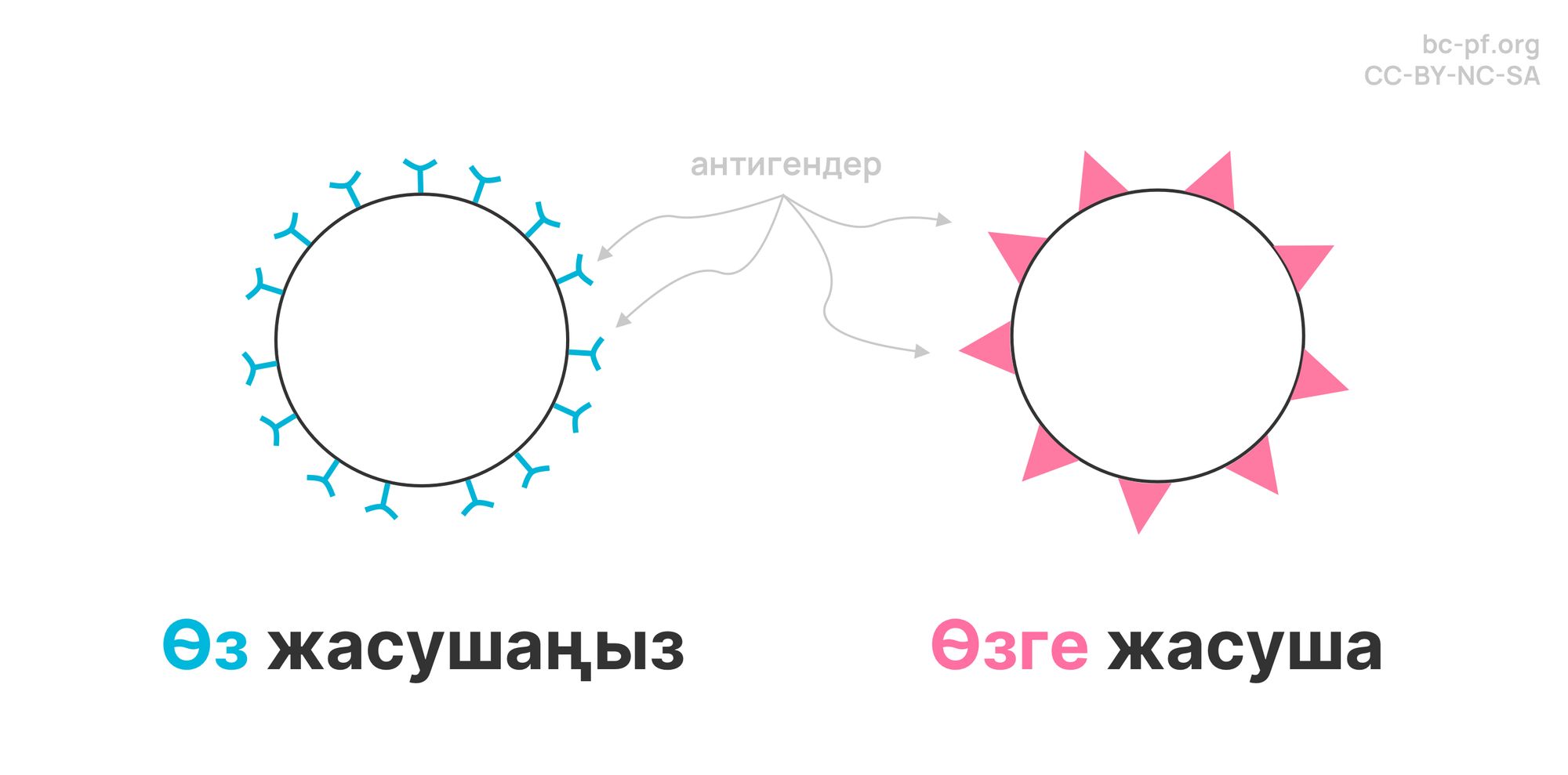
Антигендердің көмегімен. Антиген — бұл жасуша бетінде орналасқан белгілі бір молекулалық құрылым. Өз антигендеріңіз — қарапайым адам жасушаларында болатын антигендер, ал өзге антигендер — адам жасушаларында болмауы керектілер, яғни олар жергілікті (әдетте, зиянды) болып табылады. Зиянды жергілікті тұрғындарды патоген деп атаймыз.
Антигендердің гендермен ешқандай байланысы жоқ. Антиген – antibody generator (антидене генераторының) аббревиатурасы.
Және бұл жерде сұрақ туындауы мүмкін: патогендік микроорганизмдер неліктен өзін осылай ұстап беруі керек? Неліктен оларға бөгде екені туралы анық түсінік беретін антигендер қажет? Адам ағзасында олар өздерін «өзіміздікі» деп көрсетсе ақылға қонымдырақ болар еді. Бірақ олай емес. Антигендер шыршадағы сәндік ойыншықтар емес, патогеннің өмірлік циклінде сұранысқа ие функционалды элементтер екенін түсіну маңызды. Аналог ретінде зебраны пайдаланайық: егер сіз зебра аңшысы болсаңыз, онда зебра түсі сізге өте айқын болып көрінеді. Сонымен, егер сіз қара және ақ жолақтарды көрсеңіз, сіз міндетті түрде алдыңызда зебра екенін түсінесіз. Бірақ зебра үшін жолақтар жай ғана безендіру емес, сонымен бірге өте функционалды элемент: ғалымдар бұл жолақтардың қандай функцияны орындайтынын әлі дәл анықтаған жоқ, атап айтқанда, олар терморегуляцияға көмектеседі ме немесе жәндіктерді қорқытады ма екендігі белгісіз.
Сол сияқты антигендер патогендер үшін белгілі бір функцияларды орындайды. Мысалы, коронавирустың пепломері (S-ақуыз) оның адам жасушаларына енуіне көмектеседі.
Бір қызығы, туғаннан бастап әр адамның денесінде мыңға жуық түрлі антигендерді тани алатын жүзге жуық түрлі детекторлар (рецепторлар) жиынтығы бар. Бұл детекторлар туа біткен иммунитеттің негізін құрайды. Ал ол өзі кезегінде қоздырғыштардан қорғаудың бірінші желісі ретінде әрекет ететін биохимиялық реакциялар жиынтығы болып табылады.
Ал екінші жолда кім тұр? Бейімделген иммунитет. Мұнда антиденелер детекторлар ретінде әрекет етеді, олар әлдеқайда ерекше және осыған байланысты өзгермелі болады. Масштабты түсіну үшін: әртүрлі антиденелердің көмегімен \(10\) миллион түрлі антигендерді тануға болады.
№ 2. Өзге жасушаларды қалай қуып шығуға болады?
Рецептор немесе антидене антигенді танығаннан кейін, ол өзге жасушаларды жоюды бастау үшін сигнал таратады.
Туа біткен иммунитеттің сигналдарын лейкоциттер: нейтрофилдер, эозинофилдер, базофилдер, моноциттер және лимфоциттер қабылдайды. BioNinja ресурсында берілген аналогты қолданайық (сол жерде әрбір лейкоциттің егжей-тегжейлі сипаттамасы бар):
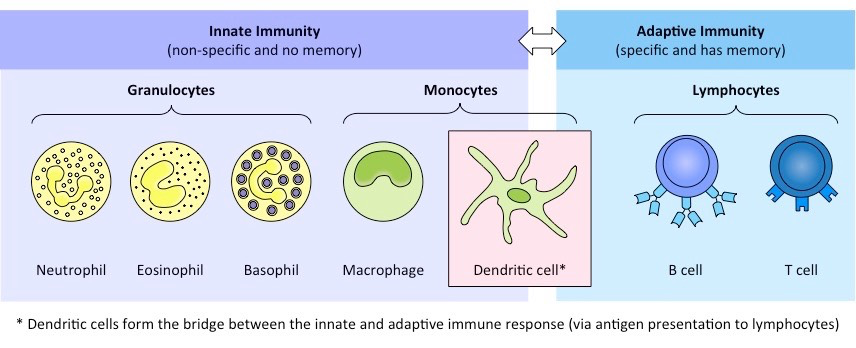
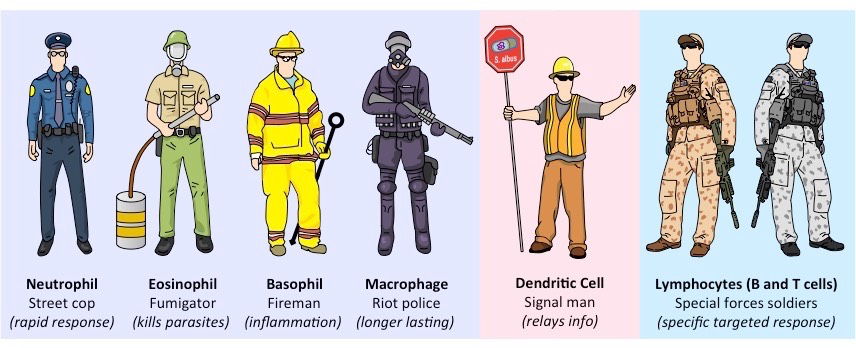
Нейтрофилдер — бұл патогенді жұтып қоюға (оны пакман сияқты жұтып қоюға) және лизосомалар арқылы оны жоюға (лизосомалар жасушаның «асқазаны» секілді) ең көп таралған лейкоцит жасушалары. Айтпақшы, сондықтан нейтрофилдер бір реттік болып табылады. BioNinja аналогында нейтрофилдер көше полициясының қызметкерлері сияқты: олар жағдайға тез әрекет етеді, бірақ арнайы дағдыларға ие емес.
Эозинофилдер аллергиялық және паразиттік инфекциялар кезінде қозадыі. Патогенді өрескел жалмаудың орнына, олар патогеннің жасушалық қабығын бұзатын молекулаларды «шашыратады». Эозинофилдер жәндіктермен күресушілер тектес (фумигаторлар).
Базофилдер — шу шығаратын ағайындылар.Олар гистамин мен гепаринді шығару арқылы қабынуды бастайды. Қабыну патогеннің таралуын тежеуге көмектеседі және оған фагоциттерді тартады.
Моноциттер екі түрлі болады: макрофагтар және дендритті жасушалар. Макрофагтар патогендерді жұтады (формальды түрде фагоцитоз деп аталатын процесс); ал макрофагтардың өзі қайта пайдалануға жарамды. Дендрит жасушалары басқа лимфоциттерге инфекция туралы сигнал береді.
Соңында, үздіктердің үздігі — лимфоциттер. В-лимфоциттері (гуморальды иммунитет аясында) және Т-лимфоциттері (жасушалық иммунитет аясында) бар. Лимфоциттердің екі түрі де иммунитетті өздері қалыптастыра алады, бірақ адам ағзасында олар өзара байланысты.
Лимфоциттер қалай жұмыс жасайды?
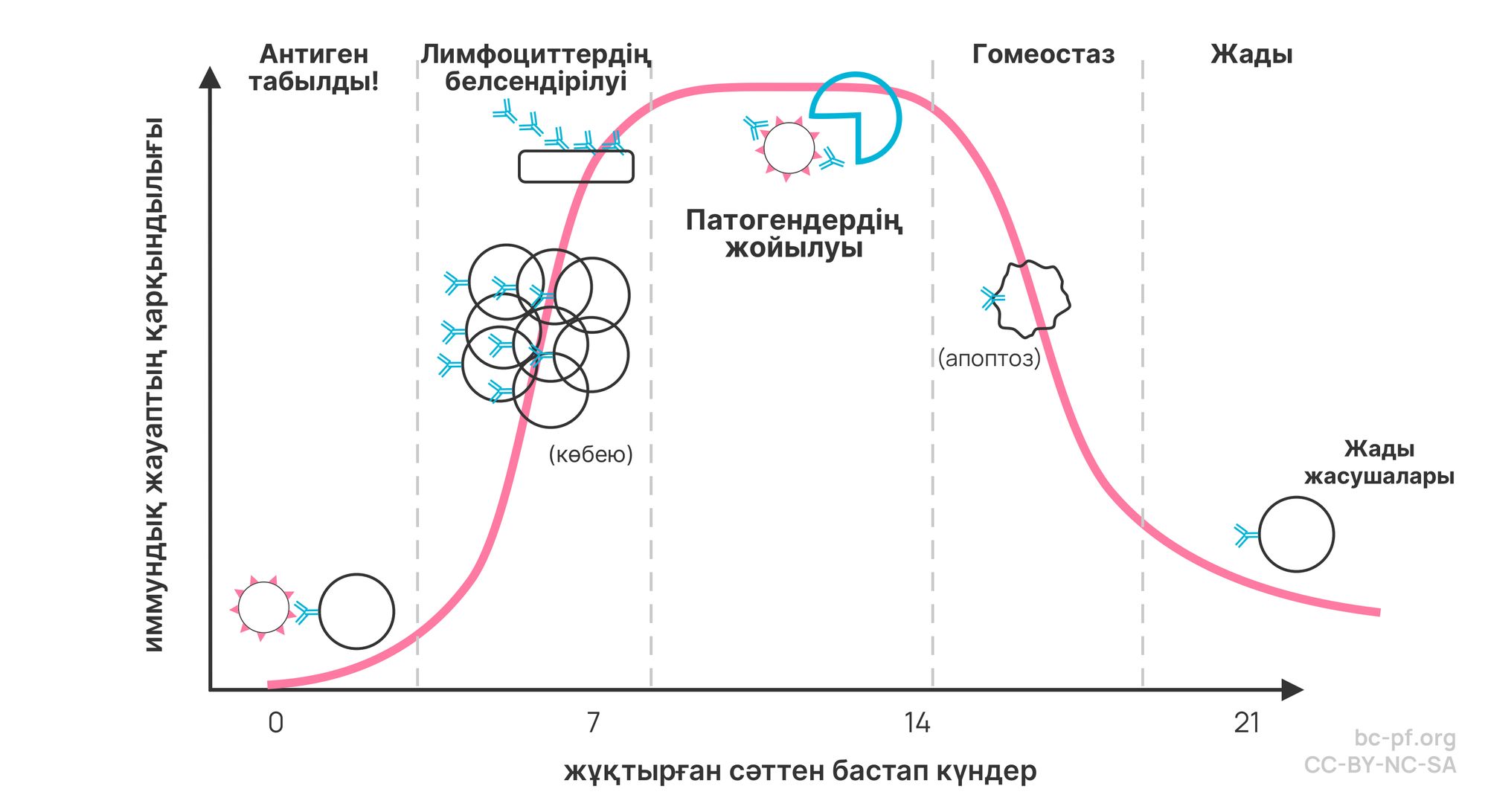
В-жасушасы
Алдымен В-жасушасымен байланысты иммундық жүйенің қалай жұмыс істейтінін қарастырайық. В жасушалары бөгде пептидтерді (ұсақ белоктарды) жұтып, оларды ыдыратады, содан кейін антигендер ретінде екінші класты негізгі гистосәйкестік кешені (MHC\(II\)) арқылы өздерінің бетіне шығарады (оларды А антигені деп атаймыз). Бетінде осы антигендер үшін рецепторлары бар Т-жасушалары осы кешенмен байланысып, CD\(40\)L молекулалары мен цитокиндерді синтездей бастайды, бұл В-жасушаларының көбеюін ынталандырады және «иммуноглобулин класының ауысуы» деп аталатын процестен өтеді. Нәтижесінде біз В жасушаларының үш түрін аламыз: плазмалық жасушалар, герминативті орталығының В жасушалары және жады жасушалары. Плазмалық жасушалар «А антигенімен» байланыса алатын антиденелердің үлкен мөлшерін синтездейді. Жады жасушалары — біз осы параграфтың басында қарастырғанмен бірдей В жасушалары. Олар да, сондай-ақ, «А антигенінің» қатысуымен белсендіріледі.
Иммуноглобулиндер класстарын ауыстыру нәтижесінде біз IgM антиденелерін шығаратын плазмалық жасушаларды және жады жасушаларын аламыз, соның ішінде IgG. Сондықтан IgM антиденелерінің болуымен аурудың қазір жүріп жатқанын, ал IgG болуы бойынша адамның біраз уақыт бұрын ауырғанын анықтауға болады.
Бірақ герминативті орталығының В-жасушаларында (ол лимфа түйіндерінде орналасқан) қызықты нәрсе болады: олар соматикалық гипермутацияға ұшырайды. Негізінен, В-жасушаларында болатын рецепторларда кездейсоқ модификациялар орын алады және осылайша көптеген көшірмелер жасалады. Әрбір көшірме «антиген А» үшін белсендірілген көмекші Т-жасушаға сай келеді және кейін байланысу сынағы өтеді: егер В-жасушасы антигенмен жақсы байланыса бастаса, онда өмір сүруге болады деген бұйрықты қабылдайды. Қарама-қарсы жағдайда апоптоз арқылы жойылу бұйрығы орын аладыі. Мұндай калибрлеу үрдісі жеткілікті жақсы байланыс алынғанша жалғасады.
Ақырында гуморальды иммундық жауапта не болады? Антиденелерді шығара алатын плазмалық жасушалар түзіледі. Бұл антиденелер белгілі бір күшпен немесе тиімділікпен «А антигенімен» байланысады. Бұл антиденелер макрофагтар патогендерді жою үшін патогендерді белгілейді. Сонымен қатар, егер антиген патогеннің өмірлік циклінде маңызды рөл атқарса, антиденемен байланысқаннан кейін патоген бейтараптандырылады. Оған қоса, иммундық жүйе болашақта антигенді ертерек, тезірек және күштірек танитындай B-жасушаларын (герминативті орталығы) калибрлейді. Сондықтан қайталанатын ауруға қарсы күшті иммундық жауап бар.
T-жасушасы
Сіздің өміріңіздің алғашқы жиырма жылында сіздің айырша безіңіз (тимус) кездейсоқ ауыстыру әдісімен мамандандырылмаған («аңғал») Т жасушаларының керемет санын жасайды. Ақырында, антиген ағзаға енген кезде дендритті жасушалар бұл антигенді алып, жас Т-жасушаларына жеткізеді. Маманданбаған Т-жасушалары белсендіріледі, көбейеді және маманданады. Кейбір Т-жасушалары В-жасушаларының жұмысын реттеуге барады (біз оларды алдыңғы бөлімде айтқанбыз). Кейбір Т-жасушалары антигенді өздігінен тауып, жұқтырған жасушаның жойылуын бастайды. Кейбір Т-жасушалары жады жасушаларына айналады. В-лимфоциттерден түзілген жады жасушаларынан айырмашылығы – бұл Т-лимфоциттердің жады жасушалары нашар зерттелген және олардың өмірлік циклі туралы ғылыми ортада әлі де пікірталастар бар.
Дененің барлық инфекцияланған жасушалары жойылғаннан кейін антиденелердің деңгейі және, тиісінше, жасушалардың плазмасы сөзсіз төмендейді. Антиденелердің аз ғана бөлігі және есте сақтау жасушаларының белгілі бір бөлігі ғана қалады. Сондықтан иммунитеттің көрсеткіші ретінде қандағы антиденелердің мөлшерін анықтау өте даулы әрекет болып табылады.
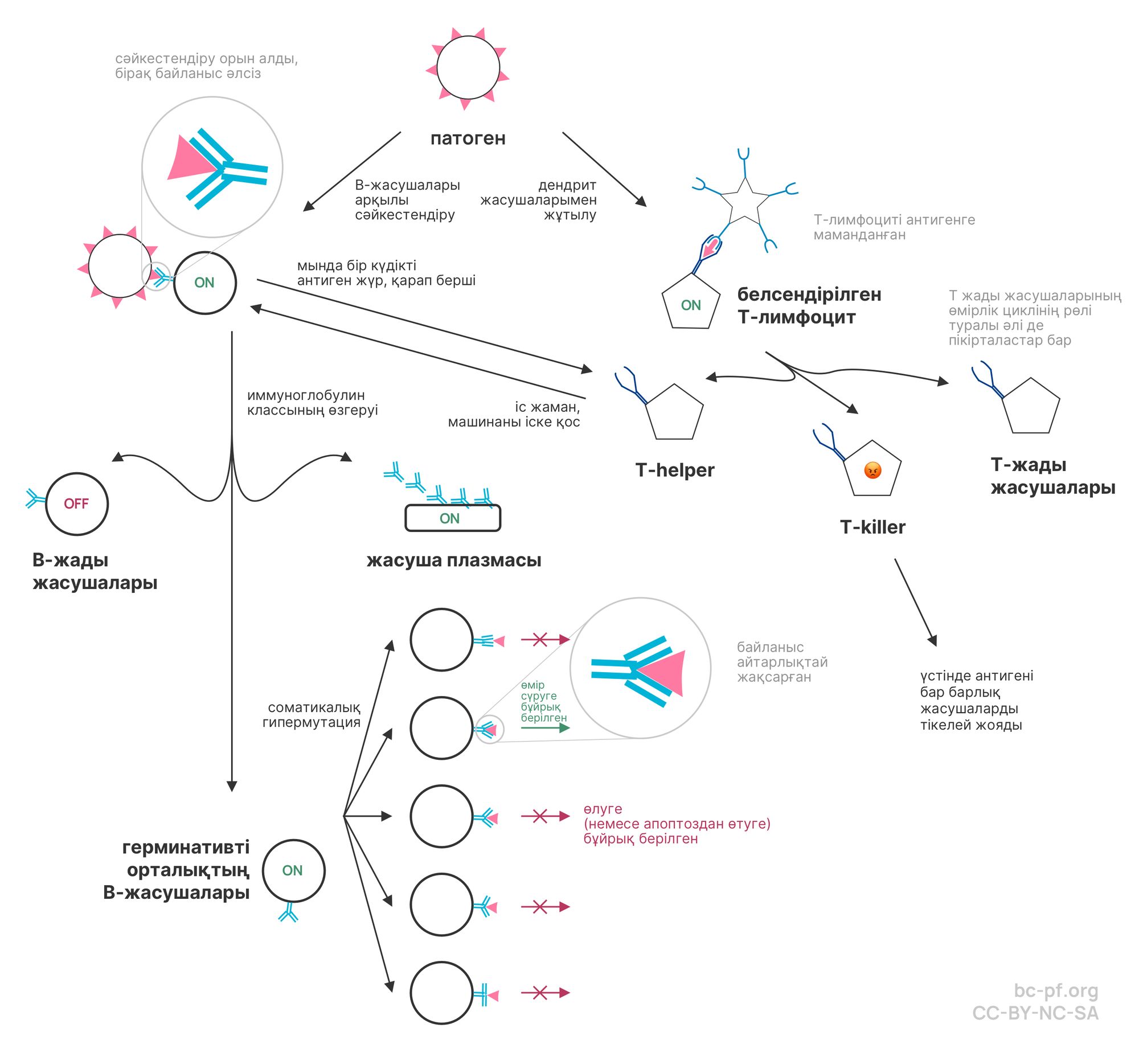
Иммундық жүйенің егжей-тегжейлі сипаттамасын оқығыңыз келсе, біздің серіктестеріміз «Биомолекуладан» материалды оқи аласыздар.
Иммунитет қалыптастыру жолдары
Осы кезде біз иммундық жүйенің бір-бірімен әрекеттесетін екі элементтен тұратынын түсіндік: өзге жасушаларды/ағзаларды белгілейтіндер және оларды жоятындар. Белгілеу көбінесе антиденелердің көмегімен жүреді. Сонымен аурумен күресудің ең жылдам жолы қандай? Антиденелердің болуы.
Олар қайдан пайда болуы мүмкін? Екі жол бар: антиденелерді ағзаның өзі шығарады немесе олар басқа біреуден дайын түрде енгізіледі. Бірінші әдіс белсенді иммунитет, екіншісі пассивті иммунитет деп аталады.
Белсенді иммунитет өз кезегінде екі түрге бөлінеді: табиғи — табиғи инфекциямен және жасанды — вакцинациямен. Басқаша айтқанда, вакцинация - антиденелердің табиғи жаратылуына барынша жақын процесс. Вакцинация кезінде біз патогеннің ағзаға өздігінен енгенін күтпейміз, бірақ оны алдын ала енгіземіз. Әдетте патоген алдын-ала әлсіреген күйде болады, ал ол жасушаларға зиян келтіре алмайды, бірақ әлі де өзге организм ретінде анықталуы мүмкін.
Пассивті иммунитет те екі түрге бөлінеді. Табиғи пассивті иммунитет ана құрсағындағы нәрестелерде қалыптасады: бала өз антиденелерін өздігінен жасай алмайтындықтан анасы оны аурулардан қорғау үшін балаға антиденелерді береді. Ал жасанды пассивті иммунитет — бұл сарысу, яғни, біз жай ғана дайын антиденелерді енгіземіз. Бұл сізге дереу әрекет ету қажет болғанда өте пайдалы (мысалы, күшті умен улану кезінде), бірақ мұндай иммунитет тез өтеді: ол бірнеше күн немесе аптаға созылады.
Қандай вакциналар болады?
Біз вакцинацияның патогенмен жасанды жұқтыру екенін түсіндік. Өзіңізді толық вируспен жұқтыру өте қауіпті болар еді. Сондықтан біз ерекше нәрсе ойлап табуымыз керек. SARS-CoV-\(2\) вакциналарының мысалын қолдана отырып, осы "шығармашылықтың" қалай көрінетінін көрейік.
Айтпақшы, ДДҰ осы тақырыпта жақсы мақала дайындады.
QazVac немесе инактивацияланған вакциналар
Қарапайым жолдан бастайық: вирусты алып, оны өлтірейік немесе сәл мейірімділік танытып, инактивациялайық. Осылайша вирус жасушаларға еніп, көбейе алмайды, бірақ антигендер әлі де оған ілініп тұрады, ал бұл иммундық жүйенің триггерлері ретінде қызмет ете алады. Көп жағдайда антигеннің рөлін коронавирусқа өз атауын беретін тікенді ақуыздар (спайк ақуыздар) атқарады. QazVac әзірлеушілерінің айтуынша, олар SARS-CoV-\(2\) вирусын қабылдап, оны формальдегидпен белсіздендіреді. Өкінішке орай, бүгінгі күнге дейін QazVac клиникалық сынақтарының екінші және үшінші фазаларының нәтижелері туралы деректер жарияланған жоқ.
Басқа инактивацияланған вакциналар: Hayat-Vax (Қазақстан Республикасында қолжетімді, БАӘ-де шығарылған, бірақ технологиясын Қытайда Sinopharm компаниясы әзірлеген, үшінші кезеңнің нәтижелері жарияланған), CoviVac (Ресейде жасалған вакцина, \(2021\) жылдың \(22\) маусымынан бастап клиникалық сынақтардың үшінші фазасының сатысында, жоспарланған аяқталу күні \(30\) желтоқсан \(2022\)), CoronaVac (Қытайда SinoVac компаниясы шығарған, жақында ДДҰ-ның төтенше рұқсатын алған және Қазақстанда таратыла бастады).
Инактивацияланған вакциналардың артықшылықтары
Жоғарыдағы жаңа ресейлік вакцина туралы біліп, сізде келесі сұрақ туындауы мүмкін: «Неге олардың ғалымдарына \(2023\) жылы ғана аяқталатын CoviVac вакцинасын сынақтан өткізуі керек? Ресейде қазірдің өзінде вакцина бар, басқасының қажеті неде? Ал біз шынымен \(2023\) жылға дейін сан-эпидтік шектеулер жағдайында өмір сүреміз бе?» Мәселен, инактивацияланған вирус ағзаға енген кезде антиденелер тек протеинге ғана емес, сонымен қатар вирустың бетіндегі басқа, мүмкін азырақ байқалатын (немесе кем дегенде талқыланатын) фрагменттерге де шығарылады. Мұның бәрі иммунитеттің күшеюіне әкеліп соқтыруы керек: вирус спайк протеинінің кейбір сыни мутациясына ұшыраса да, дене әлі де SARS-CoV-\(2\)-ге иммунитетті сақтайды. Осылайша протеинге бағытталған вакциналар вирустың экспоненциалды таралуын тоқтату үшін пандемиямен күресудегі алғашқы қару болуы мүмкін, ал инактивацияланған вакциналар SARS-CoV-\(2\) үшін соңғы соққы болуы мүмкін.
Инактивацияланған вакциналардың кемшіліктері
Егер инактивацияланған вакциналар басқаларға қарағанда тиімдірек болса, неге біз оларды әзірлеуге бар күшімізді салмаймыз? Өйткені, инактивацияланған вакциналарды жасау ұзақ, қымбат және қиын. Біріншіден, сізге бірдей коронавирусты көп мөлшерде өсіру керек, яғни қорғаныс стандарттары жоғарылатылған және тиісті жабдықпен арнайы зертхана қажет. Екіншіден, вирустың қалай әрекет ететінін және оның қандай жанама әсерлері болуы мүмкін екенін зерттеу үшін уақыт қажет.
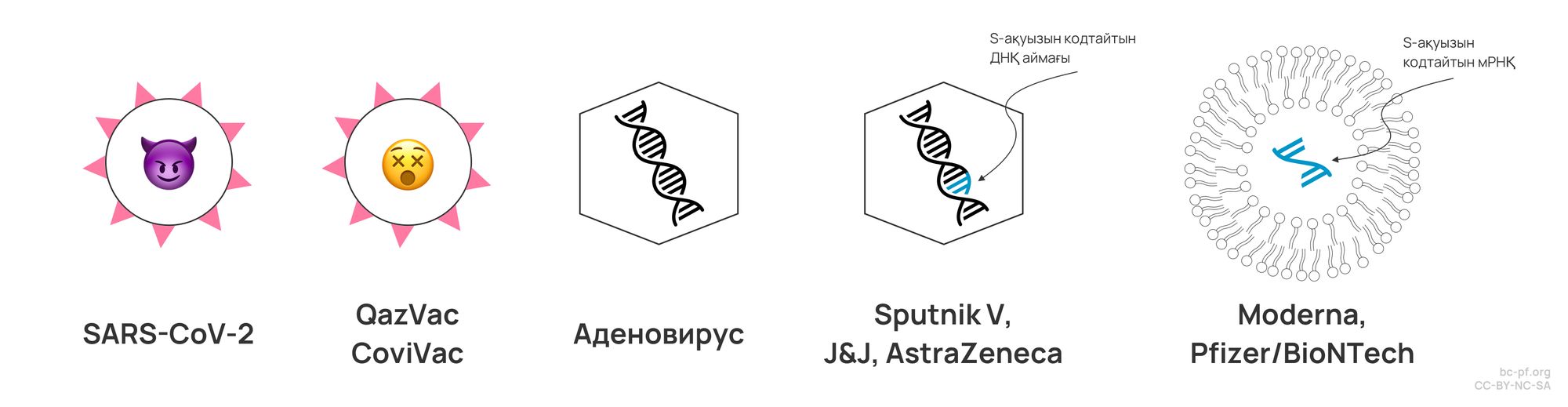
Sputnik V немесе векторлық вакциналар
Векторлық вакцинаны жасау оңайырақ және жылдамырақ. Біз не істейміз? Біз нұсқадан нұсқаға көп өзгермейтін коронавирустың кейбір фрагментін іздейміз. Бұл рөлді спайк протеині жақсырақ сомдайды: егер коронавируста спайк протеині болмаса, ол жасушаға кіре алмайды. Бұл, ең алдымен, спайк протеині әртүрлі нұсқаларда азды-көпті тұрақты болады дегенді білдіреді. Сондықтан біз осы спайк протеинін кодтайтын ДНҚ тізбегін аламыз және оны жасушаға жеткізгіміз келеді, онда осы ДНҚ-дан мРНҚ түзіледі, ол рибосомаларға спайк протеинін жасау үшін нұсқау ретінде қызмет етеді (бұл процесс молекулалық биологияның орталық догмамен сипатталады).
Қайсысы жасушаларға жақсырақ ене алады? Вирустар. Вирусты алайық, оны E1 генін алып тастау арқылы көбейту мүмкіндігінен айырайық және вирустың ДНҚ-сында (вирус – бұл капсулаға оралған ДНҚ молекуласы),спайк ақуызын кодтайтын тізбекті біріктіреміз.
Молекулярлық биологияның орталық догмасы туралы аздап толығырақ: ДНҚ белгілі бір ақуыздарды жасауға арналған нұсқауларды қамтитын генетикалық материал ретінде әрекет етеді. Транскрипция нәтижесінде бір нақты ақуызды құру алгоритмін қамтитын нұсқаулық кітапшасынан «сығулар» қалыптасады. Бұл сығулар мРНҚ болып табылады. мРНҚ-лар эндоплазмалық ретикулумға жіберіледі, онда осы нұсқауларға сәйкес ақуыз синтезі жүреді. Транскрипция және ақуыз синтезі процесі қайтымсыз: ДНҚ мРНҚ-дан жасалмайды (сирек жағдайларды қоспағанда), мРНҚ белоктан жасалмайды.
AstraZeneca, Johnson & Johnson және Sputnik V вакциналары шамамен осылай жұмыс істейді, Олардың әрбіреуінде жеткізуші ретінде аденовирустар жүреді. AstraZeneca-да бұл шимпанзеден оқшауланған ChAdOx11 вирусы, Johnson & Johnson-да Ad\(2626\) адамның аденовирусы (\(26\) дегеніміз бұл – серотип, яғни әртүрлілік), ал Спутникте – бір уақытта бірінші дозада Ad\(2626\), екіншісінде Ad\(55\).
Бірнеше сұраққа жауап берейік.
Неліктен дәл осы аденовирус?
Аденовирустар – адамға жұқтыратын ең көп таралған вирустардың бірі. Осылай әртүрлі кіші түрлер суық тиюден пневмонияға дейін ауруларды тудырады. Сондықтан аденовирустың геномы өте жақсы зерттелгені таңқаларлық емес: біз ДНҚ тізбегінің әрбір бөлімі не үшін жауапты екенін білеміз. Тұтастай алғанда, аденовирустың ДНҚ-сы жаңа ДНҚ бөлімдерінің айтарлықтай үлкен «кірістерін» орналастыра алады. Мысалы, аденовирустың ДНҚ-сында біз спайк протеинін кодтайтын тізбекті орналастыра аламыз.
Бастапқыда адам геномына бірдеңе енгізу қажет болғанда, аденовирустарды гендік терапия құралы ретінде пайдаланғысы келді. Бұл бізге не үшін керек? Генетикалық ауруларды немесе қатерлі ісіктерді емдеу үшін. Гендік терапия үшін өкінішке орай және вакцинология үшін бақытымызға орай аденовирустар адам геномына өте нашар интеграцияланады. Сондықтан, жиырма жыл бұрын аденовирустарға негізделген вакциналарды жасау бойынша белсенді жұмыс басталды. Мысалы, АИТВ-ға қарсы вакциналарды немесе туберкулезге қарсы жаңа вакциналарды жасау басталды; \(26\) аденовирусының негізінде Johnson & Johnson Эболаға қарсы вакцина жасады. Қазір аденовирустар негізінде тұмауға қарсы әмбебап вакцина жасау жұмыстары жүргізілуде (қазіргі вакциналар инактивацияланған вирустарды пайдаланады және Influenza вирусы өте тез мутацияға ұшырайтындықтан, жыл сайын жаңа вакциналар жасалуы керек).
Неліктен әртүрлі серотиптер қолданылады?
Әлем халқының \(80\)%-нан астамы аденовирустың кем дегенде бір серотипіне тап болды, соның арқасында ол осы серотипке қарсы иммунитетке ие. Осыған байланысты аденовирусқа негізделген вакцинаны пайдаланған кезде, бұл вакцинадағы жасушаларда қажетті ақуызды синтездеуге уақыттары болмауы мүмкін (мысалы, спайк), өйткені аденовирустарға иммундық реакция тез басталады және бұл жасушалар жай ғана жұтылады немесе ғылыми тұрғыдан айтқанда, фагоцитоз болады. Бір жағынан, бұл жақсы, себебі, бізде аденовирусқа қарсы вакцинасының адам ағзасында болу уақытысының табиғи шегі бар. Басқаша айтқанда, ол мәңгі болмайды:: ол ерте ме, кеш пе күйрейді. Бірақ екінші жағынан, біз вакцина жасап жатқан нәрсеге қарсы иммунитетті дамытуға уақыт болуы үшін оның ағзада болу уақытын сәл көбейткіміз келеді.
Бұл мақсатқа жету үшін сирек кездесетін серотиптерді қолдануға болады. Немесе екі түрлі болуы мүмкін, ал мұны Sputnik әзірлеушілері жасады.
Moderna және Pfizer-BioNTech
Ақуызды жеткізу үшін басқа вирусты қолдануымыз керек пе? Жоқ, бірақ біз денеге тек протеинді жеткізе алмаймыз. Неліктен? Протеин – бұл бүкіл денеге жақсы тарала алмайтын немесе қан тамырларына өздігінен енбейтін үлкен құрылым. Сонда не істеуге болады?
Молекулалық биологияның орталық догмасына жүгінсек, ақпараттың үш «кезеңі» немесе «формасы» бар екенін еске түсіреміз: ДНҚ, мРНҚ және протеиндер. Біз аденовирустар мысалында ДНҚ жеткізілімі бар нұсқаны зерттедік, протеин жеткізу нұсқасы өте қиын және мүмкін емес. Не қалды? мРНҚ.
Дәл сол мРНҚ-ны Moderna және BioNTech пайдаланған. Оның үстіне, олардың мРНҚ-сы жай ғана спайк протеинін емес, иммундық жауапты бастауға қабілетті, бірақ ақуыздың адам жасушаларына енуіне жол бермейтін белгілі бір конформациядағы спайк протеинін кодтайды. Moderna және BioNTech вакциналарының арасындағы айырмашылық осы мРНҚ-лардың жасушаларға жеткізілуінде жатыр (мРНҚ-ны жеткізу де қиын, бірақ протеиндерге қарағанда оңай).
Қызықты ескертпе: Pfizer/BioNTech вакцинасы көпшілік арасында Pfizer вакцинасы ретінде жиі аталады. Адамдарды Pfizer ұзақ тарихы бар үлкен корпорация екені жұбататын шығар. Вакцинаны шын мәнінде неміс стартапы BioNTech компаниясы ойлап тапқанын, ал Pfizer өндіруге және таратуға көмектескенін түсіну ғана маңызды. Сонымен, Moderna және Pfizer екеуі бір сұрыптан шыққан жидектер десе келеді.
Вакциналар туралы мифтер мен қате түсініктер
Бұл бөлімде біз антиваксерлердің қызуқанды сұрақтарына жауап беруге тырысамыз. Шын мәнінде, вакцинацияға қарсы тезистердің бір бөлігінен таралуының сәттілігі – бұл тезистерді ішінара ғылыми жұмыстардан алуға болатындығымен негізделген. Бірақ, әдетте, контекстен әрқашан "алып тастау" үрдісі жүреді. Сондықтан көз жекізу үшін бірге қарастырайық.
мРНҚ қандай да бір түрде ДНҚ-ға әсер ете алады ма?
Жоқ.
Біріншіден, бұл үшін мРНҚ алдымен ядролық қос мембранадан өтуі керек. Ол үшін мРНҚ-да арнайы идентификациялық элементтер болуы тиіс (тікелей айтқанда, рұқсатнама десек болады). Екі вакцинаның да мРНҚ тізбегі белгілі және ондай рұқсатнамалары жоқ.
Екіншіден, мРНҚ ДНҚ-ға айналуы үшін reverse transcriptase ферменті қажет. Бұл ферменттердің көпшілігі тек вирустарда кездеседі. Бұл олардың адам ағзасында жоқ деген сөз емес. Олар, мысалы, адам хромосомаларының теломерлерін ұзартатын теломераза кешенінде бар. Бірақ сонымен бірге бұл теломеразалар өздерінің құрамындағы РНҚ тізбегін ғана транскрипциялайды. Олар бөгде мРНҚ-ны транскрипциялай алмайды.
Үшіншіден, мРНҚ-ны ДНҚ-ға транскрипциялау бір шаруа, басқа шаруа -- бұл жаңа ДНҚ тізбегін адамның негізгі ДНҚ молекулаларына (немесе, қарапайым, хромосомаларға) енгізу. Бұл ДНҚ тізбегін енгізуге маманданған басқа фермент – интегразаны – қажет етеді. Спайк протеиндерімен байланысты бұл ДНҚ тізбегі бізге жат болғандықтан, бізде оларды ДНҚ-ға біріктіретін ферменттер жоқ екені айдай анық.
Вакцина ерітіндісінде де кері транскриптазалар немесе интегразалар жоқ екенін айтуға болады ма?
Кез келген жағдайда, сіз мРНҚ вакциналарынан қорқатын болсаңыз да, мынаны ескерген жөн:
- Оларды сізге ешкім ұсынбайды. Егер сіз мені Қазақстаннан оқып жатсаңыз, сіз физикалық тұрғыдан Pfizer/BioNTech немесе Moderna-дан вакцина жасай алмайсыз.
- Егер сіз геномыңызға вирустық РНҚ енгізуден қорқатын болсаңыз, вакцинация алуыңыз керек. Неліктен? Өйткені SARS-CoV-\(22\) коронавирусының құрамындағы РНҚ вируспен табиғи инфекция кезінде ДНҚ-ға қосылуы мүмкін екендігі туралы дәлелдер бар. Сізді коронавирустың кері транскриптаза қайдан шыққанын алаңдатады ма? Мен сізге айтатыным бұл – оның репликация үшін өте маңызды болуы. Сондықтан табиғи инфекциясы бар қол тигізбеген коронавирус сізге өте ауыр зиян келтіруі мүмкін.
мРНҚ тұрақтылығы туралы
Біреу сұрақ қоюы мүмкін: егер мен мРНҚ вакцинасын алсам, мен өмір бойы спайк протеиндерін шығарамын ба? Жоқ. мРНҚ-лар өте тез биодеградацияға ұшырайды, бұл, айтпақшы, мРНҚ вакциналарын жасаудағы мәселелердің бірі болып табылады.
Гендік терапия және аденовируске қайта оралайық
Ешкім қоймаған, бірақ әлі де жауап табуға тұрарлық сұрақ. Біз мРНҚ ДНҚ-ға қосылмайтынын түсіндік. Аденовирус ДНҚ-сы адам ДНҚ-сына қосыла ала ма? Және бір таңғаларлығы, жауап бір мағыналы «жоқ» емес. Дегенмен, үрейленбеңіз!
Біріншіден, аденовирус эписомды вектор екені белгілі. Сонымен ДНҚ хост геномына тікелей енетін вирустар бар. Сондай-ақ, жай ғана «жағында» және өз істерін табиғи жасушалық механизмдерден бөлек жасайтын вирустар да бар. Сондықтан аденовирус (әсіресе replication-defective немесе өздігінен көбейе алмайтын) хост геномына (мысалы, адамға) ене алмайтындығы туралы жалпы консенсус бар.
Дегенмен \(2010\) жылы вирустық ДНҚ-ның хост геномымен рекомбинациялану жиілігін есептеу іс жүзінде асырылған, мұнда хост тінтуірдің бауыр жасушалары болды. Міне, қызық осы жерден басталады. Егер бір көзбен қарасақ, онда 10−5 немесе жүз мыңнан бір реттік жиілікті көріп, тынышталсақ болады. Екі көзбен қарасақ, дәлірек көре аламыз:
Ересек бауырда 1011 гепатоцит бар. Интеграция жиілігі 10−5 болса да, интегралды вектор қамтитын ұяшықтардың жалпы саны 107 (он миллион) ретті болады.
Мұнда да сіз дүрбелең жасай аласыз. Сондай-ақ, оны аденовирусты вакцинацияға қарсы дәлел ретінде «кесіп тастауға» болады. Бірақ әрі қарай оқысаңыз, сол авторлар былай деп жазады:
Дегенмен, бұл деректер тәуекелді бағалауда мағыналы болуы үшін оларды бауыр жасушаларындағы өздігінен болатын мутация жиілігімен салыстыру қажет. Кеміргіштерде бұл жиілік 10−5 ретті болатыны анық. Авторлар адамдар туралы ұқсас деректерден хабардар емес. Бірақ, мысалы, гемопоэтикалық дің жасушалары (барлық қан жасушаларының антецеденттері) өте жақсы зерттелген және өздігінен пайда болатын мутациялардың жиілігі 10−4-нен 10−8-не дейін өзгереді. Нәтижесінде егер белгілі бір генге интеграциялану ықтималдығын есептейтін болсақ, онда аденовирустар үшін ол кездейсоқ мутацияға қарағанда екі есе жоғары болады, бірақ екі ықтималдық та 10−9 (немесе миллиардта бір) ретті. Дәлірек айтқанда: кездейсоқ мутациялар үшін 0.9 × 10−9 және аденовирус интеграциясы үшін 1.8 × 10−9 болмақ.
Мүмкін осы сәтте сіз өзіңізге «Не істеу керек?» деген сұрақты қоярсыз. Бұл жерде ұтымды шешім қабылдау тәуекелдерді салыстыруға негізделуі керек екенін түсіну маңызды. Өйткені, іс жүзінде ештеңе анық емес. \(100\)% тиімді және \(100\)% қауіпсіз вакцина болуы мүмкін емес.
Дегенмен, бұл вакциналар пайдасыз дегенді білдірмейді. Спутниктің үшінші кезеңінің аралық деректерін алсақ:
Вакцинаның бірінші дозасын алғаннан кейін \(21\) күннен кейін вакцинаны алған \(14964\) адамның \(16\) қатысушысында (\(0,1\)%) және плацебо алған \(4902\) адамның \(62\)-сінде (\(1,3\)%) COVID-\(19\) расталды. Нәтижесінде вакцинаның тиімділігі \(91,6\)% құрайды.
Басқаша айтқанда, \(16\) адам вакцина алғанына қарамастан ковид жұқтырған. Бірақ сонымен бірге вакцина алған адамдар үшін ауруды жұқтыру ықтималдығы \(10\) есе аз. Оның үстіне
Вакцинаны алғаннан кейін алғашқы екі апта ішінде инфекцияны жұқтырғандар арасында аурудың ауырлығы айтарлықтай ерекшеленбеді. Ал бірінші дозадан кейін \(15\) және \(21\) күн аралығында жұқтырғандар үшін орташа және ауыр COVID-\(19\) ықтималдығы \(73,6\)% төмендеді. Ал екінші дозаны қабылдағаннан кейін жұқтырғандар үшін аурудың орташа немесе ауыр болуы ықтималдығы \(100\)% төмендеді.
Сонда вакцинаны алғаннан кейін сіз әлі де оны жұқтырып, оң ПТР ала аласыз. Алайда, ауру жеңіл түрде және ауыр зардаптарсыз өтеді.
Дегенмен сізді әлі де интеграция ықтималдығы нөлге тең емес екені алаңдатады делік. Сіз таң қалуыңыз мүмкін, бірақ әр ұрпақтың өзгеруімен (яғни, шамамен \(20\)-\(30\) жыл сайын) адам ДНҚ-да \(100\)-ден \(200\)-ге дейін әртүрлі мутациялар жиналады. Сіз оны білсеңіз де, білмесеңіз де мутациялар әрқашан болады. Немесе ДНҚ-ның кем дегенде \(45\)%, шамамен жартысы транспозондардан тұратынына таң қалуыңыз мүмкін. Транспозондар дегеніміз не? Бұл ДНҚ-ның жалпы реттіліктен өз бетінше қиылып, басқа жерге кірістіруге қабілетті бөлімдері. Транспозондар эволюцияның ең күшті қозғалтқыштарының бірі болып табылады, ол қазір адам ағзасында ұйықтап жатыр және олардың ояну ықтималдығы, әрине, нөлге тең емес. Ал егер олар оянса, не болмық? Оны елестету өте қорқынышты!
Ақырында, ең болмағанда, егер сіз интеграцияның нөлдік емес мүмкіндігі туралы алаңдасаңыз, онда сіз кәуап немесе басқа гриль ет жемейсіз деп үміттенемін. Неліктен? Етті ашық отта пісірген кезде келесі процесс орын алуы мүмкін: еттен май тамшылары тамшылатып, от көзіне түседі және түтінмен бірге еттің бетіне көтеріле отырып, полициклді хош иісті көмірсутектер (PAHs) түзу үшін жанып кетедіі. PAH-мен қандай проблема бар? Олар мутагенді және канцерогенді. Басқаша айтқанда, мутациялар мен қатерлі ісік тудыруы мүмкін.
Сондағы ғибрат: «Біздің әлем әлдеқайда күрделі және түсініксіз».
Аденовирустар және АИВ
\(2020\) жылдың қазан айында сол Lancet басылымында \(5\)-серотип аденовирусына негізделген вакциналарды қолдану кезінде АИТВ-ны жұқтыру ықтималдығы жоғарылағаны туралы хат жарияланды. Және тағы да: егер сіз мұны контекстен үзіп алып оқысаңыз, дүрбелеңге түсуіңіз сөзсіз болар.
Нақты контекст қандай? \(2000\) жылдардың басында Ad\(5\) негізіндегі АИТВ вакцинасы сынақтан өтті. Анықталғандай, Ad\(5\) иммунитеті бар адамдарда АИТВ жұқтыру ықтималдығы бақылау тобына қарағанда жоғары болды. Бірақ бәрі соншалықты оңай емес. Біріншіден, мәселе \(5.1\)% Ad\(5\)-ке иммунитеті бар адамдарға қатысты және \(2.1\) туралы айтылып жатыр.
«Жанама әсерлер»
Соңында мен вакциналардың жанама әсерлері туралы айтқым келеді. Неліктен жанама әсерлер тіркесіі тырнақшаға алдым? Бұл фразамен жиі сипатталатын нәрсе – температура, бас ауруы, шаршау – мұның бәрі жанама әсерлер емес. Бұл вакцина жұмысының тікелей әсері деп айтар едім. Менің ойымша, иммунитеттің жұмысы туралы мақаланың басын оқысаңыз неге вакцинациядан кейін сіздің денеңіз вирусқа қарсы иммунитетті қалыптастыратынын түсінуіңіз керек. Қызба, бас ауруы, шаршау – бұл дененің иммундық реакциясының белгілері. Сізде бұл белгілер неғұрлым күшті болса, соғұрлым нашар нағыз коронавирус инфекциясынан аман қалар едіңіз.
Егер жаңа варианттар пайда болып жатқанда вакцинацинацияланудың қандай мәні бар ?
Жауап өте қарапайым: адамдар вакцинацияланбағандықтан жаңа нұсқалар пайда болады. Мұны тіпті математикалық түрде де көрсету оңай: мутация жиілігі – тұрақты мән. Вирустарда ол адамдарға қарағанда жоғары және \(10000\)-ға \(1\) миллионнан \(1\)-ге дейін. Егер бір уақытта миллион адам ауырса, бізді \(N\) мутация күтеді. Егер бір уақытта \(100\) миллион адам ауырса, бізді \(100n\) мутация күтеді.
Егер біреуді қызықтыратын болса: мутациялардың жиілігі генетикалық материалдың көшірілуіне жатады, яғни көшіруден өтетін \(10 000\) немесе миллион нуклеотидке бір мутация. Ал көшіру бірнеше жасушаларда болуы мүмкін, сондықтан бір ағзаның ішіндегі мутация жиілігі \(10 000\)-ға \(1\)-ден жоғары болуы мүмкін.Сол себепті барлық мутациялар функцияның күрт өзгеруіне әкелмейді, кейбіреулері, тіпті, көрінбейтін болып қалады. Сондықтан біз үшін абсолютті мутация жиіліктерін қарау өте маңызды емес: ең бастысы – ауыратын адамдардың саны көбейге сайын мутацияның біреуі өте қаупті болып, короновирустың жаңа нұсқасына алып келу ықтималдығы жоғарылайтындығын түсіну.
Қорытынды
Сонымен, біз бүгін не білдік:
- Иммунитеттің екі тұжырымдамалық бөлігі бар: біреуі бөгде бөлшектерді анықтайтын және оларды жоятын. Идентификация үшін біріншісі көбінесе антигендермен байланысатын антиденелерді пайдаланады. Аурудан (немесе вакцинациядан) кейін олардың деңгейі төмендейді, бірақ оларды жасау нұсқаулары жады жасушаларында сақталады.
- Вакциналардың жұмыс істеу механизмі табиғи инфекция механизміне өте жақын. Вакцинация -- бұл сіздің денеңіздің вирусқа қарсы қорғанысын дамытуға мүмкіндік береді.
- Ешбір вакцина \(100\)% абсолютті тиімді бола алмайды. Вакцинация инфекцияның алдын алмайды. Вакцинация сіздің жұқтырмау мүмкіндігіңізді арттырады, ал егер жасасаңыз, кем дегенде ковид жеңіл күйде өтеді .
- COVID-\(19\)-мен күресу үшін жасалған вакциналар мүлдем жаңа емес. Аденовирустар негізіндегі вакциналармен жұмыс бірнеше ондаған жылдар бойы жүргізіліп келеді. Сондай-ақ, мРНҚ-ны вакцина ретінде пайдалану \(2020\) жылдары басталған жоқ.
- Аденовирустық вакциналарды қолданумен салыстыратын болсақ, коронавирустық ауру әлдеқайда жоғары ықтималдықпен вирустық ДНҚ-ның адам ағзасына қосылуына әкелуі мүмкін. Ал аденовирустық вакциналарды қолдану кезінде интеграцияның ықтималдығы күн сайын болатын кездейсоқ мутациялардың жиілігінен сәл жоғары.
Және ең маңыздысы, қауіп деңгейін талдау кезінде олардың абсолютті мәндерін емес, оларды басқа нәрсемен салыстыру керек.
ИМХО
Соңында, рұқсат етсеңіздер, мен объективті мәлімдемелерден жеке ұстаным деңгейіне түсемін. Мен дәйекті және негізделген ұстанымы бар адамдарды құрметтеймін. Тіпті, менікіне керісінше болса да. Дегенмен өткен жылы антибиотиктерді, арбидолдарды, ингавириндерді кездейсоқ қолданған адамдар, тіпті гепарин мен дексаметазонмен соқтығысқан кезде, олардың химиялық құрамы, әрекет ету механизмі немесе қолдану қауіпсіздігі туралы ешқашан ойламаған адамдар вакциналарға қатысты өте жоғары стандарттарды орнатқан кезде мүлдем түсінбеймін (біз \(100\)% қауіпсіздік пен \(100\)% тиімділікті қалаймыз). Бәлкім, өзіңізді алдап, медицинаны түсінемін деп жүруді қоярсыз? Сіз, тіпті, бактериялар мен вирустардың айырмашылығын түсінбейсіз немесе аңғармайсыз.
Адамдардың бактериялар мен вирустардың айырмашылығын түсінбеуі сөздік қорында да көрінеді. Сіз коронавирустың «дельта штаммы» деген тіркесті жиі естідіңіз бе? Және бұл мүлдем дұрыс емес. Вирустарға қатысты «вариант» деген дұрыс. Мысалы, «дельта вариант».
Біреу вакцинацияны әркімнің жеке таңдауы деп ойлайды. Жарайды, бұл сіздің таңдауыңыз болсын. Бірақ емханада орын жеткіліксіз болған кезде немесе жедел жәрдем ұзақ уақыт жүрсе, сіз басқаларды кінәлауды бастамаңыз – бұл сіздің таңдауыңыздың салдары. Дүние жүзіндегі бірде-бір денсаулық сақтау жүйесі, тіпті, халқының \(30\)%-ының бір мезгілде келуіне төтеп бере алмайды. Есіңізде болсын, әрбір таңдаудың салдары болады. Кез келген таңдау және кез келген еркіндік жауапкершілікпен келеді. Ал біріншісін шынымен пайдаланғыңыз келсе, екіншісіне дайын болыңыз.
P.S.
Б.А.Загрибельный мен Адылхан А.Қ. шолуларды және ғылыми дәлдікке тексергені үшін алғысымды білдіргім келеді
Аударған: Әнел Есбергенова
Редактор: Дильназ Жемісбек
